NEWSお知らせ
【研究成果】光合成タンパク質の単一分子計測〜蛍光揺らぎが雄弁に語る光合成の調節機構〜
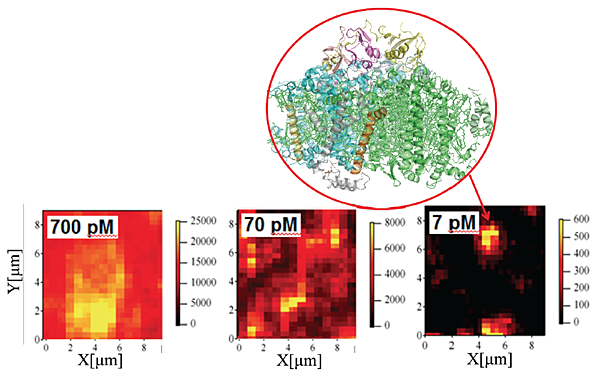
下の3つの図は、光化学系Ⅰの濃度を薄くしていったときに極低温顕微鏡観察で観測されたイメージ。
7 pMまで薄くすることで、一つ一つの光化学系Ⅰ分子が粒として見えてきた。
研究の背景
1つの分子からの蛍光を測定する単一分子観測技術は、2014年のノーベル化学賞の対象にもなった技術で、近年ますます発展して広い科学分野で使われています。そもそも1つの分子を見ると何が嬉しいのか?いろいろなメリットがありますが、その一つに、たくさんの分子を観測していると隠れてしまって見えなくなる分子の揺らぎを見ることができるようになることがあります。例えば、森の木々は1本1本違うはずですが、森全体を遠くから眺めるとそれぞれの個性は見えません。1本1本の木を個々に見ることで、それぞれが異なる揺れ方をしたりするのが見えてきます。同じように、たくさんの分子から発せられる蛍光は強度が一定でその色も一定ですが、1つの分子を見るとその蛍光の強さが時間とともにふらふらするブリンキングと呼ばれる現象や、蛍光波長(色)が時間とともに変動するようなことが起こることが、単一分子計測から見えてきました。
このような揺らぎは、蛍光を発している分子の周りの環境が変動していることに由来すると考えられています。化学反応が実際に起こるためには揺らぎが必要ですが、単一分子蛍光計測の適用により初めて多くの種類の分子で、実際に化学反応に重要となる揺らぎが観測できるようになってきたのです。
単一分子からの蛍光を計測するには、サンプルの濃度を極端に薄くして、顕微鏡の対物レンズで集光されるレーザー光のスポットサイズ(波長の半分くらい、約0.3 ㎛)に分子が1個以下になるようにします。こうして、レーザーの集光点には分子が1個しかない状況を実現し、その分子からの蛍光を同じ対物レンズで集めて検出します。別の分子を測定する場合は、レーザーの集光位置を変えて別の分子を見つけます。
私たちは、光化学系Ⅰ(注1)と呼ばれる光合成で働くタンパク質について単一分子計測技術を適用することを目指して、極低温でも動作する顕微鏡開発を行ってきました。図1は、濃度を薄くした光化学系Ⅰサンプルを極低温顕微鏡で観測したイメージで、黄色く見えている粒子が一つの光化学系に対応します。光合成で働くタンパク質は、室温では光合成の最初の化学反応である光による電子移動反応(注2)が非常に高効率で起こるため、蛍光はほとんど出ません。そのため、光化学系で単一分子計測を行うためには、どうしても極低温での測定を行う必要があったのです。
研究成果
開発した極低温顕微鏡の写真を図2に示します。市販の顕微鏡とは見た目が全然違っていて、接眼レンズはありません。サンプルの透過像はカメラを使ってモニターします。サンプルはカバーガラスで密閉され、内部が真空になる銀色の大きな筒状のサンプル室(図2右)内に設置されて極低温にまで冷える銅製のロッドにつなげられます。サンプル室を真空にするのは、魔法瓶で保温するのと同じ原理によりサンプルを極低温に保つためです。サンプルをつないだ銅製ロッドに液体窒素を流すことで、約80 K(-193℃)までサンプルは冷やすことができます。
今回開発した顕微鏡では、対物レンズを真空のサンプル室内に設置することで、顕微鏡の性能を向上することができました。断熱性の高い真空中に設置することで対物レンズは室温に保たれるため、高い性能の極低温顕微鏡とすることができたのです。
一方で、室温に保たれた対物レンズのすぐ傍に液体窒素の温度にまで冷やされたサンプルホルダがあることから、少しの手違いで両者が接触して高価な対物レンズを破損してしまう危険性があります。そのようなことのないように、対物レンズとサンプルホルダの距離が近づくと音が鳴るアラームを設置して、常に細心の注意をもって実験行う必要があります。
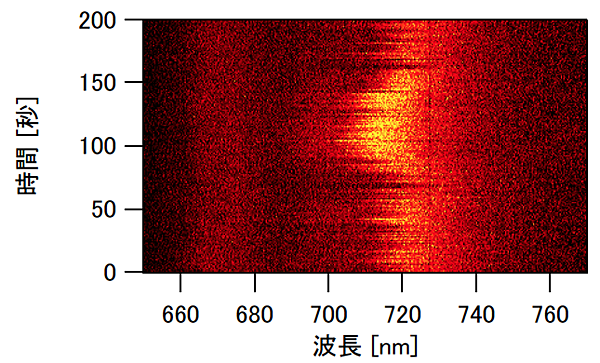
対物レンズの性能向上のおかげで、光化学系Ⅰの1つ1つを図1右側のイメージに見られるような明るい粒々として見られるようになりました。レーザーの焦点をある光化学系Ⅰ分子の場所に固定してその分子の蛍光スペクトルの時間変化を測定する実験を行ったところ、蛍光のブリンキングや蛍光波長の揺らぎが見られることを発見しました。その一例を図3に示しています。この図の横軸は蛍光の波長を示しています。ある光化学系Ⅰ分子1つにレーザーの焦点を集光して、その分子からの蛍光スペクトルを1秒おきに200秒間測定し続けました。図3の縦軸は測定した時刻を表します。蛍光の強度が不規則に揺らいでいるのと同時に、蛍光が強くなる波長(横軸方向の位置、蛍光の色に対応)も時間とともに揺らいでいるのが分かります。
たくさんの分子を観測していると絶対に見ることのできないこのような不思議な現象を、初めて光化学系Ⅰという光合成のタンパク質に対して観測することができました。光化学系Ⅰは、図1に示したような構造をしていることが分かっています。1つの光化学系Ⅰタンパク質には、葉緑素クロロフィル(注3)が約100個結合しています。この100個のクロロフィルの大部分は、光エネルギーを集めるアンテナとして機能しており、タンパク質のほぼ中心にある反応中心クロロフィル(P700と呼ばれる)(注4)に光エネルギーを渡します。
現在のところ、タンパク質の構造の小さな変化によって光化学系Ⅰ内部の光エネルギーの流れる経路が変化することによって、蛍光強度の揺らぎや色の揺らぎが起こっていると考えています。図4に模式的にその様子を表しています。どのような構造変化が起こっているかは今のところ謎です。光合成を行なうタンパク質は、通常は高い効率で光エネルギーを化学エネルギーに変換する反応を行っていますが、光が強すぎる状況では光反応の効率が高いと活性酸素などの有害な物質を生成してしまい、細胞を死なせてしまう危険があります。このように光が強すぎる場合には、クロロフィルが吸収した光エネルギーを熱として安全に捨てて有害物質が蓄積しないようにする機構があることが知られています。今回の単一分子計測で見えてきたブリンキングが、このような光エネルギーを集める効率の調節機構と関係があるかもしれないと考え、研究を続けています。
発表雑誌
この研究は東北大学の柴田穣准教授、福村裕史教授らの研究グループと名古屋大学の野口巧教授の研究グループの共同により行われました。研究成果は2014年3月17日にElsevier社の学術雑誌である『Biochimica et Biophysica Acta』1837巻に掲載されました。
Yutaka Shibata, et al. "Development of a novel cryogenic microscope with numerical aperture of 0.9 and its application to photosynthesis research" Biochim. Biophys. Acta, 2014, 1837, 880-887
参考図

左が全体で、右はサンプルが収まる真空チャンバーの内部。
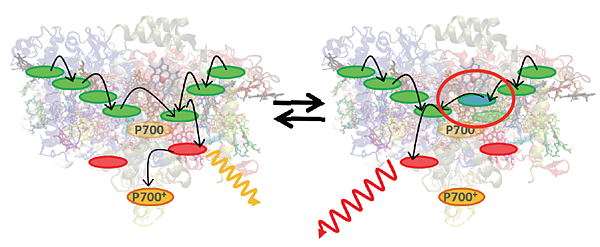
緑、オレンジ、赤の楕円がクロロフィルを表す。オレンジで表したクロロフィルが反応中心P700を表す。
赤色の楕円で示すクロロフィルから蛍光が発する。
右側の青色の楕円の位置が変化することで、エネルギーの流れが変化したことを模式的に表している。
用語解説
(注1)光化学系Ⅰ
植物や藻類などの酸素を発生する光合成において、光エネルギーを化学エネルギーに変換する働きをするタンパク質が2つあるが、そのうちの1つ。
(注2)電子移動反応
電子がある物質から別の物質に移動する反応。光合成では、光を吸収したクロロフィル分子から別の分子への電子移動反応により、光エネルギーが化学エネルギーに変換される。
(注3)クロロフィル
光合成で働く色素分子の名前。植物では主にクロロフィルaとクロロフィルbという2種類のクロロフィルが働いている。光化学系Ⅰにはクロロフィルaが約100個結合している。
(注4)反応中心クロロフィル
光化学系Iなどの光合成タンパク質で、光エネルギーを使った電子移動反応が起こるクロロフィル分子のこと。光化学系Ⅰの反応中心クロロフィルは、700 nmの光を吸収することが知られており、P700と呼ばれる。P700から電子が移動したのちは、正イオンとなりP700+となる。
お問い合わせ先
東北大学大学院理学研究科 化学専攻
准教授 柴田 穣(しばた ゆたか)
電話:022-795-6568
E-mail:shibata[at]m.tohoku.ac.jp
*[at]を@に置き換えてください
Posted on:2017年1月17日





