お知らせ

- トップ
- お知らせ
細胞の血行性転移の新たな仕組みを発見
世界初、新たながん転移抑止戦略の開発にも期待
ポイント
● がん疾患を最も高い死因に押し上げている要因は、がん細胞が転移を行うという性質。血管中のがん細胞の多くがどうして毛細血管から血管外へと遊出するかが不明だった。
● 転移細胞が血管外に遊出するためには、はじめに細胞が自身の硬さを利用して毛細血管に「挟まる(つまる)」ことで血管にとどまる必要があることを世界で初めて発見。
● 細胞の硬さを操作対象とする、がん細胞転移の新たな抑止戦略につながることが期待。
概要
がんが人類最大の死因である原因は、がん細胞は血管を移動路として使用して活動の場を全身に広げる、いわゆる「血行性転移(以降、転移)(※1)」を行う性質によるものです。血液中を循環するがん細胞の多くは毛細血管から血管の外へと遊出することは知られていましたが、毛細血管からの遊出が起こりやすい原因についてはあまりわかっておらず、その仕組みの解明が望まれていました。
今回、血中を流れる細胞が血管の外への遊出を行うために、毛細血管のところで「ブレーキ」をかける新たな転移の仕組みを解明しました。
九州大学大学院理学研究院の齋藤大介教授、寺本孝行准教授の研究グループは、京都大学の高橋淑子教授、東北大学の田村宏治教授と船本健一准教授、名古屋大学の宮田卓樹教授、東京農工大学の吉野大輔准教授、岡山理科大学の田所竜介准教授、明海大学の長坂新助教、同志社大学の城所比奈子助教との共同研究で、転移する細胞モデルとしてニワトリ胚の生殖細胞を用いた解析を行い、転移細胞が血中で硬くなることで細い血管に「挟まって(つまって)」しまうことを世界で初めて明らかにしました。すなわち、細胞が血管の外に遊出する場所を確保するために、細胞が自身の「硬さ」を「ブレーキ」として用いていることを突き止めたわけです。
今回の発見は、細胞の硬さを操作対象とする、がん細胞転移の新たな抑止戦略につながることが期待されます。 本研究成果は米国の雑誌「iScience」に2022年11月28日(月)に掲載されました。
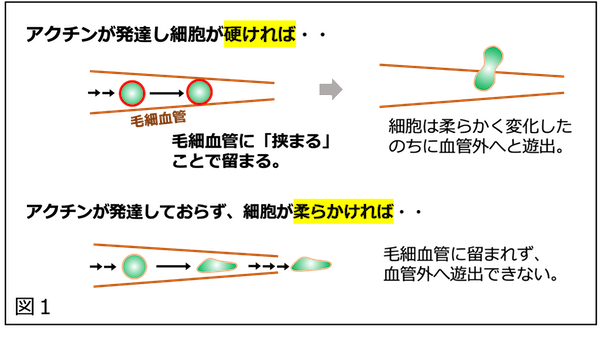
図1 今回の発見の概要
転移可能な細胞では細胞膜直下に繊維状アクチンが発達しており、このため高弾性である(硬い)。この硬さゆえに細い流路(毛細血管)にて「挟まって」移動を停止する。停止した細胞はこの血管領域から遊出する(上図)。一方で繊維状アクチン形成を阻害した場合、細胞は柔らかくなり毛細血管にて「挟まる」ことができなくなり、結果として血管外遊出ができない。
研究の背景と経緯
がんは人類にとって死因第一位の疾患です。この疾患を深刻たらしめている原因は、細胞が血管を移動路として使用して遠隔に移動できる性質、いわゆる細胞の「転移能」です。転移によってがん細胞は活動の場を全身に広げ、そこで無秩序に増殖分化して臓器不全が引き起こされることで死に至ります。そのため、がん克服には転移機構の理解が極めて重要です。
転移は「細胞の血管への侵入、血管内での循環移動、移動先での血管外への遊出」と複数のプロセスから構成されますが、特に最後の「血管外への遊出プロセス」はあまりわかっていません。理解が深まらない大きな理由の一つに、このプロセスを生体の中で実際に視ることの難しさがあります。細胞の遊出は体内深部にて、高速で起こる現象である上に、どこでそれが起こるかが予想できないのが問題なのです。もちろん個体を殺してしまえば断面化するなどして細かく視ることはできますが、そうすると細胞の動きは全くわからなくなります。このように、細胞が血管から遊出する様を観察したくてもそれが難しいのが現状でした。そこで、この現象を効率的に高解像度で観察・解析でき、できれば血管内を流れる一つ一つの細胞までつぶさに観察できる、優れた生体モデル系が必要とされていました。
研究の内容と成果
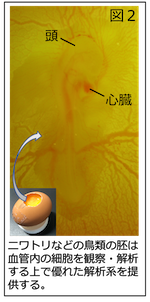 鳥類の生殖細胞(※2)は胚の時期、血管の中を移動路として用いて移動するという、転移性がん細胞と同様にふるまうとても興味深い細胞です。我々の研究から、鳥類とその生殖細胞の血管内でのふるまいが、細胞の血管外への遊出を解析する上で優れたモデルとなることがわかってきました。鳥類の生殖細胞が血行性移動(転移)をする発生時期は決まっていて、ニワトリでは孵卵2-3日目に起こります。この時期の胚は平板状の比較的単純な構造をしており、血管網全体を余すことなく顕微鏡で詳細に観察できます(図2)。しかも、生殖細胞はその血管網の中でも、いつも決まったタイミングで特定の毛細血管から遊出することまで見出しておりました。
鳥類の生殖細胞(※2)は胚の時期、血管の中を移動路として用いて移動するという、転移性がん細胞と同様にふるまうとても興味深い細胞です。我々の研究から、鳥類とその生殖細胞の血管内でのふるまいが、細胞の血管外への遊出を解析する上で優れたモデルとなることがわかってきました。鳥類の生殖細胞が血行性移動(転移)をする発生時期は決まっていて、ニワトリでは孵卵2-3日目に起こります。この時期の胚は平板状の比較的単純な構造をしており、血管網全体を余すことなく顕微鏡で詳細に観察できます(図2)。しかも、生殖細胞はその血管網の中でも、いつも決まったタイミングで特定の毛細血管から遊出することまで見出しておりました。
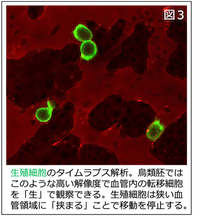 我々はこの優れた解析系を用いて細胞の血管外遊出機構の研究を進めました。はじめに生殖細胞を蛍光色素で見えるようにして観察すると、生殖細胞が特定の毛細血管にて突然循環を停止することがわかりました。そこは後に生殖細胞が血管の外に遊出する毛細血管でした。生殖細胞がどのようにしてこの場所に停止するのかを明らかにするためにさらに詳細なタイムラプス解析(※3)を行ったところ、多くの生殖細胞はその特定の毛細血管領域まで流れてくるとその血管に挟まってしまうことがわかってきました(図3)。しかし、赤血球など他の細胞たちは挟まらずに血管の狭い領域をすり抜けて流れ去っていくため、「どうして生殖細胞だけ挟まってしまうのか」が次の疑問となりました。次に我々は、「生殖細胞は硬く、硬いからこそ血管に挟まって止まるのではないか」と仮説を立てました。結論としてこの仮説は正解でした。まず、原子間力顕微鏡(※4)という物体の硬さ(弾性)を計測できる装置で生殖細胞の硬さを測定したところ、生殖細胞は血球細胞よりも4倍も硬いことがわかりました(赤血球と比較すると8倍も硬い)。さらに、生殖細胞にこのような強度を与えている物質が、細胞表面を裏打ちするアクチン(※5)と呼ばれるタンパク質であることもわかってきました。重要なことに、生殖細胞においてこのアクチンの機能を低下させると、細い通路にて挟まることができずにすり抜けて流れ去ってしまうことがわかりました。これはマイクロ流路デバイス(※6)を用いた解析から明らかとなりました。以上の研究から、転移細胞の血管の外への遊出には、細胞の「硬さ」が必要であることが示されたわけです。
我々はこの優れた解析系を用いて細胞の血管外遊出機構の研究を進めました。はじめに生殖細胞を蛍光色素で見えるようにして観察すると、生殖細胞が特定の毛細血管にて突然循環を停止することがわかりました。そこは後に生殖細胞が血管の外に遊出する毛細血管でした。生殖細胞がどのようにしてこの場所に停止するのかを明らかにするためにさらに詳細なタイムラプス解析(※3)を行ったところ、多くの生殖細胞はその特定の毛細血管領域まで流れてくるとその血管に挟まってしまうことがわかってきました(図3)。しかし、赤血球など他の細胞たちは挟まらずに血管の狭い領域をすり抜けて流れ去っていくため、「どうして生殖細胞だけ挟まってしまうのか」が次の疑問となりました。次に我々は、「生殖細胞は硬く、硬いからこそ血管に挟まって止まるのではないか」と仮説を立てました。結論としてこの仮説は正解でした。まず、原子間力顕微鏡(※4)という物体の硬さ(弾性)を計測できる装置で生殖細胞の硬さを測定したところ、生殖細胞は血球細胞よりも4倍も硬いことがわかりました(赤血球と比較すると8倍も硬い)。さらに、生殖細胞にこのような強度を与えている物質が、細胞表面を裏打ちするアクチン(※5)と呼ばれるタンパク質であることもわかってきました。重要なことに、生殖細胞においてこのアクチンの機能を低下させると、細い通路にて挟まることができずにすり抜けて流れ去ってしまうことがわかりました。これはマイクロ流路デバイス(※6)を用いた解析から明らかとなりました。以上の研究から、転移細胞の血管の外への遊出には、細胞の「硬さ」が必要であることが示されたわけです。
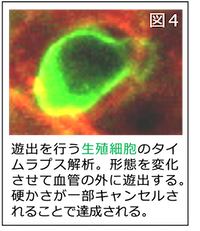 最後に、生殖細胞が毛細血管に挟まった後に起こるイベントである、血管の外への遊出も調べました。循環中の「硬い」生殖細胞はほぼ球形の形をしているのですが、毛細血管に挟まるとすぐに形を大きく変化させて血管の壁をすり抜けることがわかりました(図4)。この遊出時に見せる細胞の構造が、アクチン機能が低下した細胞で見られる特徴的な構造であったことから、遊出時には生殖細胞は「柔らかく」なると推察されます。つまり、転移細胞は自分の硬さを巧みに調節することで血管外への遊出を達成することもわかってきました。
最後に、生殖細胞が毛細血管に挟まった後に起こるイベントである、血管の外への遊出も調べました。循環中の「硬い」生殖細胞はほぼ球形の形をしているのですが、毛細血管に挟まるとすぐに形を大きく変化させて血管の壁をすり抜けることがわかりました(図4)。この遊出時に見せる細胞の構造が、アクチン機能が低下した細胞で見られる特徴的な構造であったことから、遊出時には生殖細胞は「柔らかく」なると推察されます。つまり、転移細胞は自分の硬さを巧みに調節することで血管外への遊出を達成することもわかってきました。
今後の展開
今回、生殖細胞の転移における細胞の「硬さ」の重要性が明らかになりました。今後、血液内を循環しているがん細胞も「硬い」のか、早急に調べる必要があります。もしがん細胞も硬いのであれば、がん転移抑止の新たな方法として、細胞の硬さの操作が有効になり得ます。がん転移をターゲットとした戦略が乏しい現状においては画期的な方法になる可能性があります。また、細胞が血流の中でどうして硬くなるのか(アクチンが発達するのか)はこれから調べていきますが、その仕組みが明らかになれば転移抑制に向けたまた新たな医療戦略が創出されます。
用語解説
(※1) 血行性転移
がん細胞などが血管へ侵入し、血流循環に乗って遠隔まで移動し、血管の外に遊出するプロセスを含む細胞移動
(※2) 生殖細胞
精子や卵、それらの元となる細胞。胚の時期の生殖細胞は始原生殖細胞と呼ばれる。始原生殖細胞は胚の外で生まれ、発生の間に体内に作られる生殖腺まで移動する。鳥類の場合、その移動路として胚の血管も利用している。
(※3) タイムラプス解析
画像ではなく映像を取得する解析。生きている個体や細胞の動きを解析する上で効果的。
(※4) 原子間力顕微鏡
操作型プローブ顕微鏡の一種。顕微鏡に付属したプローブを物体に押し込む解析を行うことで、物体の弾性測定に応用できる。今回はプローブで細胞を押し込んでいる。
(※5) アクチン
細胞骨格と呼ばれる、細胞の構造を支えるタンパク質の一種。
(※6) マイクロ流路デバイス
透明なシリコン等で形成された人工水路。今回は毛細血管を模して10μm幅の流路を設計し、その中を実際の血流と同じ速度で細胞を流して解析を行なった。
謝辞
本研究はJSPS科研費 (JP23116705, JP25111719, JP15K14358, 18H02445, JP20K21425, JP20H03259, JP 19H04775)、内藤記念科学奨励金・研究助成、ひと・健康・未来研究財団研究助成、武田科学振興財団ライフサイエンス研究助成、成茂動物科学振興基金の助成を受けたものです。
論文情報
掲載誌:iScience
タイトル:Stiffness of primordial germ cells is required for their extravasation in avian embryos
著者名:Daisuke Saito, Ryosuke Tadokoro, Arata Nagasaka, Daisuke Yoshino, Takayuki Teramoto, Kanta Mizumoto, Kenichi Funamoto, Hinako Kidokoro, Takaki Miyata, Koji Tamura and Yoshiko Takahashi.
DOI:10.1016/j.isci.2022.105629
問い合わせ先
<研究に関すること>
東北大学大学院生命科学研究科、理学部生物学科[web]
教授 田村 宏治(たむら こうじ)
TEL:022-795-3489
E-mail:tam[at]m.tohoku.ac.jp
<報道に関すること>
東北大学大学院生命科学研究科 広報室
TEL:022-217-6193
Mail:lifsci-pr[at]grp.tohoku.ac.jp
*[at]を@に置き換えてください
Posted on:2022年12月13日