お知らせ

- トップ
- お知らせ
神経細胞の膜環境を変化させる新たな仕組みの発見
〜分泌タンパク質リーリンによる神経細胞膜の脂質組成制御〜
研究成果の概要
名古屋市立大学 大学院薬学研究科の服部光治教授、東北大学 大学院生命科学研究科の田口友彦教授、慶應義塾大学 薬学部・理化学研究所・横浜市立大学 生命医科学研究科の有田誠教授、ストラスブール大学の小林俊秀教授らの研究グループは、神経細胞の膜環境を制御する新しい仕組みを発見しました。本研究成果は国際神経化学会(International Society for Neurochemistry)が発行する雑誌Journal of Neurochemistryに2025年9月3日に公開されました。
研究のポイント
● 分泌タンパク質「リーリン」(注1)が、神経細胞膜上のスフィンゴミエリン(SM)(注2)量を増加させることを発見。
● SM量増加に伴い、特定の膜タンパク質の細胞膜上量が増加する。
● リーリン欠損マウスの脳内では、SM合成に関わる脂質分子の組成が野生型と比較して異なる。
背景
神経細胞の細胞膜は多種多様な脂質分子によって構成されます。その中でもSMは、細胞膜上に様々なタンパク質の局在や機能を調節する「場」を形成する重要な脂質です。ゆえにSMは神経細胞の機能に不可欠であると考えられています。しかし、神経細胞膜においてSMの量がどのように制御されているのかは不明でした。
研究グループはこれまでに、主に中枢神経系に存在する分泌タンパク質リーリンが、脳の脂質組成制御に関わること(Mizukami et al., 2018)、また、リーリンシグナルの下流分子の活性化によって、非神経細胞の膜上SM量が増加すること(Baba et al., 2009)を報告してきました。以上より、リーリンは神経細胞膜のSM量制御に関わることが考えられました。
研究の成果
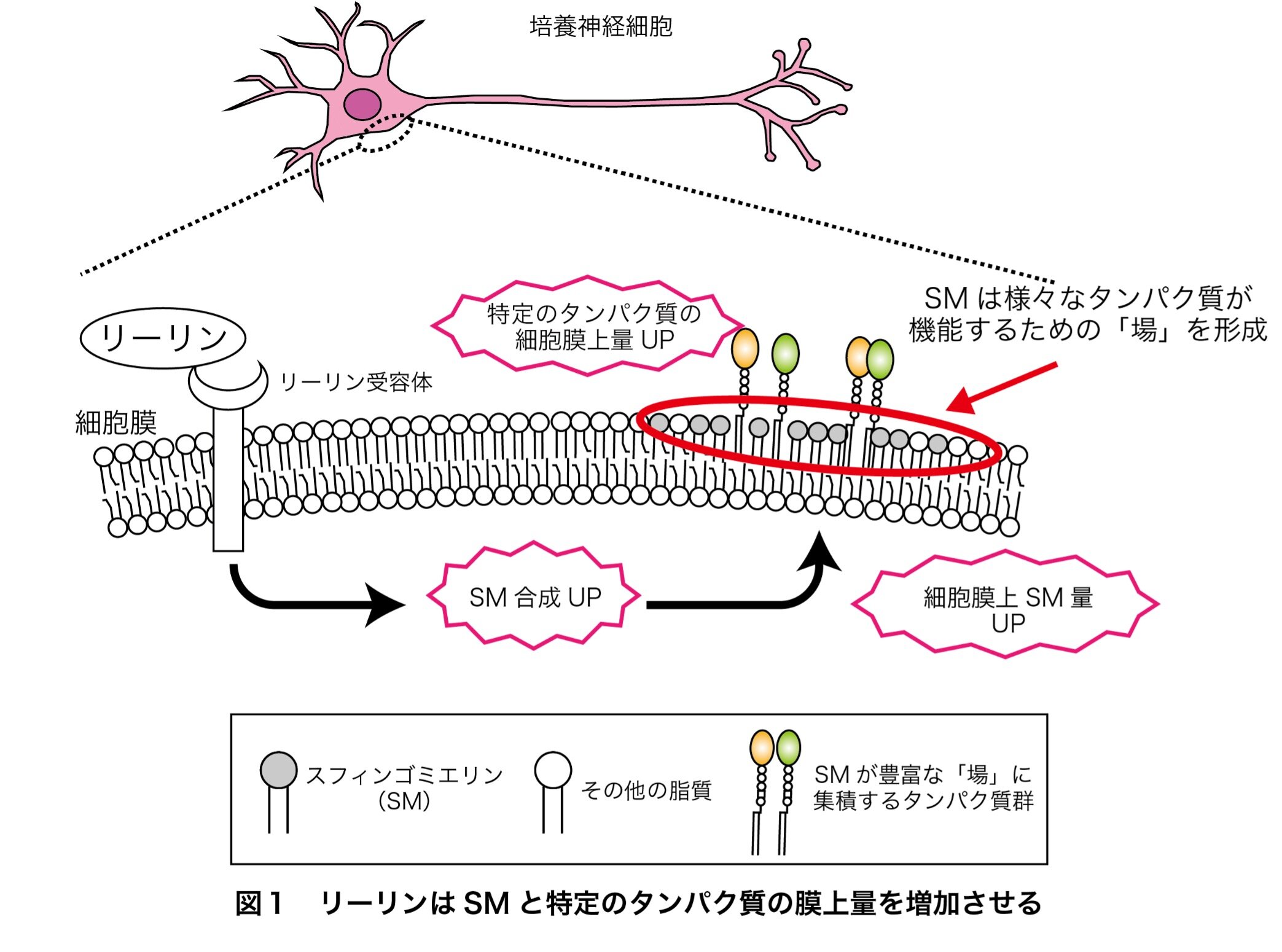
今回の研究では、海馬由来の培養神経細胞にリーリンを添加することにより、細胞膜上のSM量が増加することを発見しました。このリーリンの効果は、神経細胞のSM合成能を向上させることを介することを見出しました。さらに、リーリンはSMを増加させるとともに、SMによって形成される「場」に集積する、特定のタンパク質の膜上量も増加させることを発見しました。また、脳から抽出した神経細胞膜由来の画分を解析した結果、リーリン欠損マウスではSM合成の材料となるセラミドとホスファチジルコリンの割合が高く、SM合成能の低下が示唆されました。以上より、リーリンは神経細胞膜上のSM量を制御し、特定のタンパク質の局在にも影響を与える因子であることが明らかになりました。
研究の意義と今後の展開や社会的意義など
アルツハイマー型認知症を含む神経変性疾患では、脳内のSMの量が減少することが報告されています。本研究成果は、神経細胞膜のSM量制御機構の理解を深めるとともに、将来的には細胞膜脂質制御に注目した病態の解明や、これを標的とした新しい神経変性疾患の治療法の開発につながることが期待されます。
用語解説
注1. リーリン:主に中枢神経系に存在する分泌タンパク質であり、脳の構造形成、神経細胞の形態形成、神経細胞間情報伝達の調節など、様々な機能を持つ。
注2. スフィンゴミエリン(SM):主に細胞膜に存在する脂質分子であり、細胞膜の構造維持やシグナル伝達に重要な役割を果たす。
研究助成
本研究は、文部科学省科学研究費助成事業(JP24KJ1889 竹腰祐斗、JP20H03384およびJP23K27324 服部光治)、名古屋市立大学卓越研究グループ支援事業(2401101)、公益財団法人テルモ生命科学芸術財団(服部光治)、文部科学省先端研究基盤共用促進事業(コアファシリティ構築支援プログラム)(JPMX0441500025)、JST SPRING (JPMJSP2130)の支援を受けて行われました。
論文情報
タイトル:Reelin increases the sphingomyelin content of the plasma membrane and affects the surface expression of GPI-anchored proteins in hippocampal neurons
(リーリンは海馬神経細胞において、スフィンゴミエリン量とGPI-アンカー型タンパク質の細胞膜上量に影響を与える)
著 者:竹腰 祐斗1、安藤 飛悠吾1、河野 孝夫1、高瀬 弘嗣2、田口 友彦3、有田 誠4,5,6,7、小林 俊秀8、服部 光治1*
所属
1、名古屋市立大学 大学院薬学研究科
2、名古屋市立大学共用機器センター
3、東北大学 大学院生命科学研究科
4、理化学研究所 生命医科学研究センター
5、横浜市立大学 大学院生命医科学研究科
6、慶應義塾大学 薬学部
7、慶應義塾大学 世界トップレベル研究拠点プログラム
ヒト生物学―微生物叢―量子計算研究センター(Bio2Q)
8、ストラスブール大学 薬学部
(*Corresponding author)
雑誌名:Journal of Neurochemistry(ジャーナル オブ ニューロケミストリー)
DOI:10.1111/jnc.70225
引用文献
Mizukami T, Ikeda K, Shimanaka Y, Korogi K, Zhou C, Takase H, Tsuiji H, Kono N, Kohno T, Arai H, Arita M, Hattori M (2018) Reelin deficiency leads to aberrant lipid composition in mouse brain. Biochem Biophys Res Commun 505: 81-86.
Baba A, Akagi K, Takayanagi M, Flanagan J G, Kobayashi T, Hattori M (2009) Fyn tyrosine kinase regulates the surface expression of glycosylphosphatidylinositol-linked ephrin via the modulation of sphingomyelin metabolism. J Biol Chem 284: 9206-14
問い合わせ先
<研究に関すること>
東北大学大学院生命科学研究科 兼担 理学部生物学科[web]
教授 田口 友彦
TEL: 022-795-6676
Email: tomohiko.taguchi.b[at]tohoku.ac.jp
<報道に関すること>
東北大学大学院生命科学研究科広報室
高橋 さやか(たかはし さやか)
TEL:022-217-6193
Email:lifsci-pr[at]grp.tohoku.ac.jp
*[at]を@に置き換えてください
Posted on:2025年9月12日