お知らせ

- トップ
- お知らせ
エンベロープウイルス粒子を検出するサンドイッチELISAを実現 ―脂質膜結合性リガンドの利用により「タンパク質」検出を「ウイルス粒子」検出に変換―
発表のポイント
● 生化学において標的の検出や定量に広く用いられているサンドイッチELISA(注1)に適用可能な脂質膜結合性検出リガンド(注2)を開発し、A型インフルエンザウイルス(IAV)粒子の検出を実現しました。
● 通常の抗体型検出リガンドとは異なり、遊離タンパク質(注3)には一切応答せず、IAV粒子を特異的に検出するため、ウイルス粒子の機能(感染力)評価が可能です。
● 併用する抗体やDNAアプタマー(注4)を変更することで様々なウイルス粒子計測にも有用です。
概要
A型インフルエンザなど、ここ10年ほどの間に世界的に大流行したウイルス感染症のほとんどは、脂質膜を持つウイルス(エンベロープウイルス)によるものです。ウイルスによる感染症拡大抑制対策にはウイルス解析技術が必要不可欠であり、一般的にはウイルス粒子内に含まれるタンパク質を計測する抗体法ならびにゲノム(核酸)を計測するPCR法が用いられています。一方、これらはウイルス粒子構造を破壊後に解析する手法であり、感染力などのウイルス粒子としての機能を評価することは困難です。
東北大学大学院理学研究科の佐藤雄介准教授らの研究グループは、典型的なエンベロープウイルスであるA型インフルエンザウイルス(IAV)粒子を解析するための新たな分析技術を開発しました。佐藤准教授らが独自に開発してきたウイルス脂質膜に結合する両親媒性α-helixペプチド(AHペプチド)(注5)をサンドイッチELISA法の検出リガンドとして用いることで、IAV粒子の選択的検出を実現しました。本手法は原理上様々な種類のエンベロープウイルスに適用可能であり、ウイルス粒子の機能解析や感染力評価などへの展開が期待できます。
本研究成果は、2026年4月2日(米国東部時間)にアメリカ化学会(ACS)の学術誌ACS Sensorsに掲載されました。
詳細な説明
研究の背景
ここ10年ほどの間に局所的・世界的流行を引き起こしたウイルス感染症のほとんどは、脂質膜を持つウイルス(エンベロープウイルス)によるものです。ウイルス解析技術は感染症拡大抑制対策において必要不可欠であり、一般的にウイルス粒子に内包されているタンパク質を計測する抗体法やゲノム(核酸)を計測するPCR法が用いられています。これら既存技術はウイルス感染症診断に有用であるものの、いずれもウイルス粒子を破壊した後にその成分を計測することに基づいているため、ウイルス粒子としての機能を解析することは容易ではありません。粒子構造を破壊せずに機能解析できれば、ウイルス粒子の機能、たとえばウイルスの感染力を評価することが可能になると期待できます。
東北大学大学院理学研究科の佐藤雄介准教授と西澤精一教授の研究グループは、名古屋大学大学院医学系研究科の佐藤好隆准教授との共同研究により、ウイルス粒子表面の高曲率性脂質膜に結合する両親媒性α-helixペプチド(AHペプチド)を基盤とする蛍光応答性プローブの開発を進めてきました(Anal. Chem., 2025, 97, 5480-5487.)。このAHペプチド型蛍光プローブはエンベロープウイルス粒子選択的に応答し、簡便かつ迅速な蛍光検出が可能です。しかし、原理上様々な種類のエンベロープウイルスに応答してしまうため、特定の種類のエンベロープウイルスを選択的に解析することは困難でした。
今回の取り組み
本研究グループは、生化学で汎用されているサンドイッチELISAに着目し、IAV表面の膜タンパク質HAを認識するDNAアプタマーを修飾した基盤とAHペプチドを併用することで、IAV粒子選択的な検出技術を開発しました(図1)。サンドイッチELISAは基板上に修飾したリガンドで標的分子を捕捉した後に、もう一つの酵素が連結した検出リガンドでサンドイッチ型複合体を形成させ、酵素反応により標的分子を検出します。
一般的にサンドイッチELISAはタンパク質を検出対象としますが、研究グループは検出リガンドとして、AHペプチドを利用することで、ウイルス粒子構造を特異的に解析できるのではないかと考えました。その結果、アポリポプロテイン(Apolipoprotein) A-IのC末端領域のAHペプチドを短縮化したtrApoCと長鎖アルキル鎖(C12)を結合部位としたリガンド(trApoC-C12 : 図2)が有用な検出リガンドとして機能することを見いだしました。これにより、基板上にてDNAアプタマー/IAV粒子/trApoC-C12のサンドイッチ型複合体が形成され、trApoC-C12にあるbiotinとストレプトアビジン(SA)による相互作用を介して連結した酵素HRP(西洋ペルオキシダーゼ)による呈色反応(基質TMBの酸化反応)が起こり、発色・検出を行うことができます(図1)。様々な種類のエンベロープウイルスとの比較から、本手法はDNAアプタマーによるIAVの選択的な捕捉により、IAVの選択的な検出が可能であることを実証しました(検出限界(LOD):4.5 × 105 TCID50/mL(注6))。また、一般的なELISAで用いられる抗体を検出リガンドとして用いた場合とは異なり、本手法ではHAタンパク質には一切応答しないことを実証しました。これは検出リガンドのtrApoC-C12部位がIAV粒子選択的な結合能を有しているためであり、これによりIAV粒子特異的なサンドイッチELISA解析が可能であることを意味しています。
この性質を利用することで、本技術はIAV粒子の機能、すなわちウイルス感染力評価にも適用可能です。事実、感染力の異なるIAVサンプルを用いた評価から、本技術により推定される感染力は細胞変性効果(CPE)(注7)観察による一般的な分析手法と高い相関を示しました。
さらに、trApoC-C12にペプチド核酸(PNA)を連結したリガンドを合成し、trApoC-C12によるウイルス脂質膜結合とPNAを介したHybridization chain reaction(HCR)(注8)とを融合することで、IAVに対する検出感度が3.4倍向上することを見出しました(LOD:1.3 × 105 TCID50/mL)。本手法の検出感度は市販されているIAV解析キットと同程度であり、IAV感染診断に適用しうる実用性も有しています。
今後の展開
本研究で開発した分析技術は、IAV粒子の構造や機能解析など基礎研究に加えて、IAV感染症の診断・予防・治療などへの応用が期待されます。本手法は一般的な生化学で用いられるサンドイッチELISAに基づいているため、多くの研究者がすぐに利用できる利点があります。さらに標的ウイルス種類に適したDNAアプタマーや抗体を利用することで、様々なエンベロープウイルス解析にそのまま適用し得るプラットフォームになると期待できます。
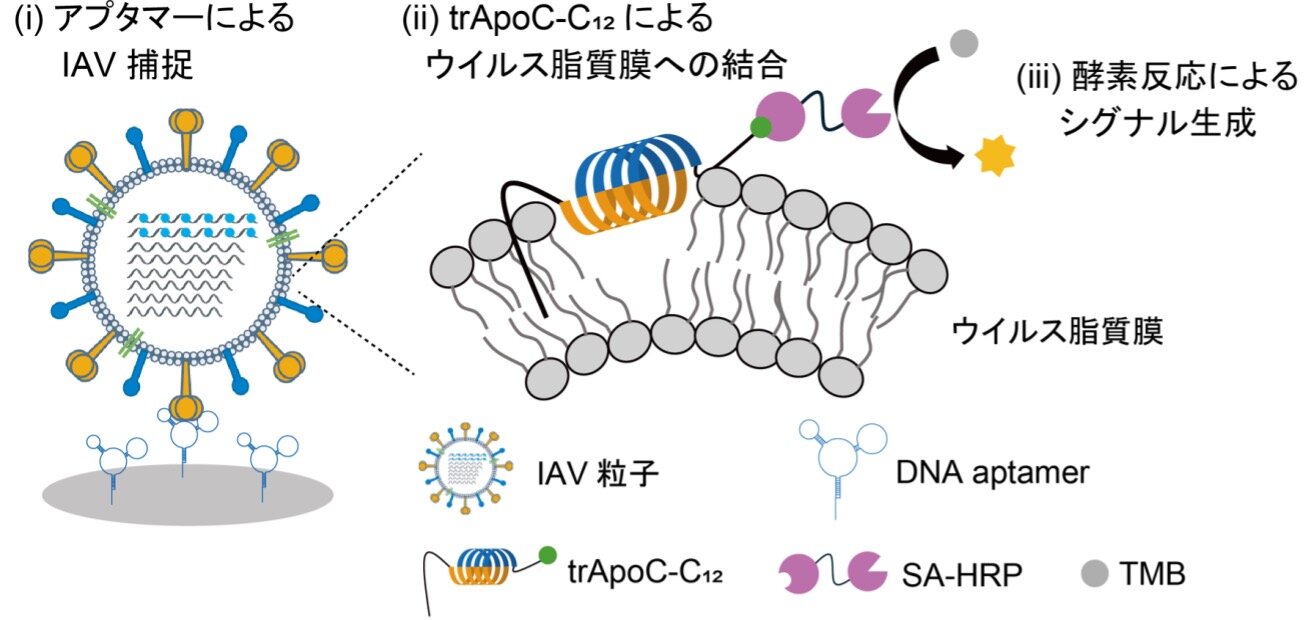
図1. 本手法の概略図:(i) 基板に固定化したHAを認識するDNAアプタマーによるIAV捕捉、(ii) ウイルス脂質膜に結合するtrApoC-C12リガンドへの結合(iii) HRP部位によるTMB酸化反応による発色・検出
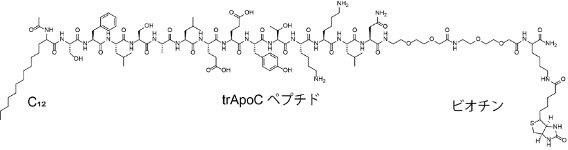
図2. trApoC-C12の構造式
謝辞
本研究は、科学技術振興機構(JST)創発的研究支援事業(JPMJFR236J)、日本学術振興会(JSPS)科学研究費助成事業(JP23H00297)の支援を受けて行われました。本論文は『東北大学2025年度オープンアクセス推進のためのAPC支援事業』によりOpen Accessとなっています。
用語説明
注1. サンドイッチELISA:2種類の分子により、標的を挟み込んで(サンドイッチ)複合体を形成させ、標的を検出・定量する方法。一般的には結合分子として抗体を用いることが多く、検出用抗体の先に連結した酵素による呈色反応を用いる(ELISA:enzyme-linked immunosorbent assay、酵素結合免疫吸着測定法)。
注2. 脂質膜結合性検出リガンド:ウイルス粒子表面の脂質膜に選択的に結合する分子(リガンド)。リガンドに酵素を連結することで、酵素反応による検出が可能。
注3. 遊離タンパク質:ウイルス粒子を構成していたタンパク質が、粒子の破壊などに伴って水中に遊離したもので、感染力はない。
注4. DNAアプタマー:特定の標的分子に対して優れた結合能を有する機能性DNA。
注5. α-helixペプチド(AHペプチド):α-helix構造を取った際に、疎水面と親水面が生じるペプチド配列。両親媒性α-helix ペプチドの中には、その疎水面が高い曲率を持つ脂質二重膜の表面に現れる脂質パッキング欠損構造に挿入(疎水性挿入)される性質を持つものがある。
注6. TCID50/mL:1mL中における50%の培養細胞を死滅させうるウイルス量。
注7. 細胞変性効果(CPE):ウイルスの侵入・感染により引き起こされる宿主細胞の形態変化。
注8. Hybridization chain reaction(HCR):特定の一本鎖DNAとこれに結合するヘアピン型DNA2種類による連続的な二重鎖形成により長いDNA二重鎖が形成される反応。
論文情報
タイトル:Viral membrane-targeting amphipathic helical peptide ligands for colorimetric sandwich assays of influenza A virus particles
著者:Kota Matsumoto, Yusuke Sato*, Yusaku Hatanaka, Satoshi Kurihara, Yoshitaka Sato, Arihiro Narita, Seiichi Nishizawa*
*責任著者:東北大学大学院理学研究科 准教授 佐藤雄介、教授 西澤精一
掲載誌:ACS Sensors
DOI:10.1021/acssensors.6c00241
問い合わせ先
<研究に関すること>
東北大学大学院理学研究科化学専攻[web]
准教授 佐藤 雄介(さとう ゆうすけ)
TEL:022-795-6551
Email:yusuke.sato.a7[at]tohoku.ac.jp
<報道に関すること>
東北大学大学院理学研究科 広報・アウトリーチ支援室
電話: 022-795-6708
E-mail:sci-pr[at]mail.sci.tohoku.ac.jp
*[at]を@に置き換えてください
Posted on:2026年4月 6日